English
ЗАКОН ДЕЙСТВУЮЩИХ МАСС
Суть закона действующих масс (закона действия масс) состоит в том, что скорость химической реакции пропорциональна концентрации реагирующих веществ в степенях, равных стехиометрическим коэффициентам этих веществ в уравнении реакции. Для реакции
nAA + nBB + ... → nCC + nDD + ...
закон действующих масс запишется следующим образом:
v = 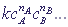 , где
, где
cA, cB, ... - концентрации реагирующих веществ A, B, ... ;
nA, nB, ... - порядки реакции по соответствующим реагентам (как правило, совпадают со стехиометрическими коэффициентами этих реагентов в уравнении реакции);
k - коэффициент пропорциональности, константа скорости реакции, зависящая от природы реагирующих веществ и от температуры;
v - скорость реакции.
Данное уравнение носит название кинетического уравнения реакции.
В состоянии термодинамического равновесия концентрации всех реагирующих веществ, согласно закону действующих масс, связаны соотношением (константа равновесия):
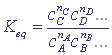
Концентрация твердого вещества в процессе химического превращения не меняется (процесс идет на поверхности), поэтому скорость в реакциях с участием твердого тела определяется только концентрацией газов или растворенных веществ.
В сложных (многостадийных) реакциях скорость всего процесса зависит от скорости наиболее медленной реакции.
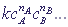 , где
, где