ОБЗОРЫ
Ризниченко Г.Ю. "КЛАССИЧЕСКИЕ МОДЕЛИ КЛЕТОЧНЫХ ПРОЦЕССОВ"
Вся биологическая жизнь происходит в клетках. Живые организмы представляют собой
либо отдельные клетки, либо многоклеточные образования. Простейшей живой системой является бактериальная клетка.
Рассматривая клетку в электронный микроскоп, можно увидеть в ней особые макромолекулы - длинные цепи сложной формы из сотен атомов. Во всех клетках обнаруживаются два рода таких макромолекул - белки и нуклеиновые кислоты (ДНК и РНК).
В бактериальной клетке имеется два типа белков - ферменты, действующие как катализаторы различных метаболических процессов, и структурные белки, являющиеся ее строительным материалом. В клетках высших организмов имеется также множество других белков,
выполняющих специальные функции - антитела иммунной системы, гормоны и др.
Клеточные процессы генетически управляемы. Синтез ферментов, которые управляют метаболизмом, управляется генами. Молекулы РНК переносят от ДНК необходимую
для синтеза ферментов информацию и устанавливают связь между генетическими и метаболическими характеристиками клетки. Такая система регуляции придает клеточным процессам чрезвычайную устойчивость. В последние годы расшифрованы информационные
последовательности геномов многих организмов, а также установлена пространственная
структура огромного количества различных белков.
Мембраны
Важнейшее свойство клетки как целостной системы - наличие границы - клеточной мембраны. В области, отгороженной от внешней среды этой границей, происходят процессы клеточного метаболизма, который обеспечивает жизнедеятельность клетки. Жидкость внутри клеточной мембраны называется цитоплазмой, а клеточная
мембрана - цитоплазматической мембраной. Большинство клеток имеют также жесткую клеточную стенку, или оболочку.
Мембрана представляет собой липидный бислой с встроенными молекулами белков,
она постоянно находится в активном состоянии - открывается и закрывается, впуская одни вещества внутрь и выпуская другие наружу. Вся деятельность мембраны направлена на поддержание клетки как отдельной сущности и защиту от вредных внешних воздействий.
Существование мембраны - необходимое условие жизни клетки. Именно мембрана придает клетке индивидуальность и позволяет в течение всей своей жизни поддерживать необходимые условия для протекания метаболических процессов.
Все ядерные клетки и большинство бактерий обладают также внутренними мембранами,
ограничивающими внутреннюю среду клеточных органелл - ядра, митохондрий, хлоропластов в фотосинтезирующих клетках и других. Все мембраны клетки объединены в единую мембранную структуру - эндомембранную систему.
Метаболизм
В цитоплазме клетки, ограниченной мембраной, происходит сложный непрерывный биохимический процесс, в ходе которого посредством химических реакций и энергетических потоков клетка непрерывно производит, ремонтирует и производит самое себя. Этот
процесс называется метаболизмом. Продукты одних реакций являются субстратами
для других, образуя цепи метаболических реакций, замкнутые цепи называются циклами.
Цепи имеют точки разветвления - реакции, продукты которых могут быть использованы не в одной, а в нескольких метаболических цепях. Таким образом, метаболические процессы представляют собой сети.
Метаболической сети клеток свойственна совершенно особая динамика, кардинально отличающая ее от внешней неживой среды. Получая продукты питания извне, клетка поддерживает себя при помощи сети происходящих внутри цитоплазматической мембраны химических реакций, производя таким образом все клеточные компоненты, в том числе и саму мембрану.
По-видимому, динамика самовоспроизводства и составляет ключевую характеристику живого. Определение живой системы как автопоэтической сети означает, что феномен жизни - это свойство системы в целом. В соответствии с этим определением вирусы
не являются живыми, так как не обладают собственным метаболизмом. Для производства новой вирусной частицы, согласно инструкции, закодированной в его (вируса) ДНК, нужно добавить метаболизм живой клетки-хозяина.
Даже у простейших метаболическая сеть чрезвычайно сложна. Большинство процессов ускоряются ферментами и происходят с использованием энергии высокоэнергетических фосфорсодержащих молекул АТФ и других высокоэнергетических соединений. При помощи транспортных РНК сеть каталитических реакций и энергетическая сеть АТФ связаны с геномом (клеточными молекулами ДНК), который сам является сложной сетью, где гены прямо или косвенно регулируют работу друг друга.
Сеть, охватывающая метаболизм, энергетику и генетический уровень, называется
эпигенетической сетью (epi, греч. - "над"), она осуществляет производство макромолекул
из метаболитов и осуществляет самовоспроизводство автопоэтической сети в целом.
В своей деятельности эпигенетическая сеть постоянно сталкивается с физическим и химическим давлением со стороны окружающей среды. Непрерывное взаимодействие с внешней средой является необходимым условием жизни. Понимание особенностей физических и химических процессов, протекающих внутри живой системы и на ее границе с окружающей средой так же важно для понимания основ жизни, как понимание биологических генетических информационных программ, реализуемых при репликации
ДНК. Сочетание физико-химических и информационных процессов в эпигенетических сетях и составляют сущность живого.
Клетка как динамическая система
Все клеточные структуры далеки от термодинамического равновесия. Метаболизм
клетки с помощью непрерывного потока энергии постоянно восстанавливает элементы
структуры по мере их распада. Удаленность от термодинамического равновесия с точки зрения кинетического подхода означает нелинейность уравнений, описывающих систему. Живые системы организационно замкнуты (представляют собой автопоэтическую сеть), но через них проходит непрерывный поток вещества и энергии. Клетки непрерывно поглощают пищу, отфильтрованную мембраной, и производят шлаки. Будучи встроены в организм, клетки могут производить также важные для других клеток организма
вещества. Этот круговорот материи определяет место клетки в окружающей среде.
С точки зрения теории динамических систем клетка является диссипативной
структурой. По определению И.Р.Пригожина, диссипативная структура - это открытая
система, которая поддерживает себя в термодинамически неравновесном, но структурно
устойчивом состоянии за счет потоков вещества и энергии. Термин "диссипативная"
подчеркивает, что поддержание структуры требует затраты (диссипации) энергии.
Специфической чертой диссипативных структур является способность к спонтанному
возникновению новых форм порядка. При возрастании потока энергии система может
прийти в точку неустойчивости, называемой "точкой бифуркации", после прохождения
которой система может пойти по совершенно другому пути, допускающему возникновение
новых структур и упорядоченных форм.
Теория динамических систем, развитая первоначально для описания физических и
химических процессов, описываемых системами нелинейных дифференциальных уравнений,
оказывается полезной для понимания самых общих качественных свойств живых систем.
Это хорошо понимал один из крупнейших математиков 20 века Тьюринг, озаглавивший
свою математическую работу, посвященную исследованию свойств системы двух нелинейных
дифференциальных уравнений с диффузией "Химические основы морфогенеза". К таким
фундаментальным свойствам относятся способность функционировать в двух или нескольких
стационарных режимах, периодически менять свои характеристики, образовывать
пространственно неоднородные структуры. Все эти свойства могут быть получены
при рассмотрении относительно простых базовых моделей математической биологии.
БАЗОВЫЕ МОДЕЛИ КЛЕТОЧНОЙ БИОЛОГИИ
Рассмотрим математические модели отдельных процессов, протекающих в клетке. Это очень простые модели, допускающие аналитическое исследование. Эти модели были предложены разными авторами в разное время. Их объединяет то, что на каждой из этих моделей удалось показать качественно важные свойства, присущие процессам в живых системах.
Фермент-субстратная реакция Михаэлиса-Ментен
Схема базовой ферментативной реакции предложена Михаэлисом и Ментен в 1913 г.
Она может быть представлена в виде:
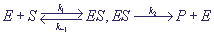 (1) (1)
Схема означает, что субстрат S соединяется с ферментом E в комплекс ES, в котором
происходит химическое превращение, и который затем распадается на фермент E
и продукт P. По закону действующих масс, скорость реакции пропорциональна произведению
концентраций. Обозначив концентрации реагентов малыми буквами: s = [S], e = [E], c = [ES], p = [P], получим систему уравнений:
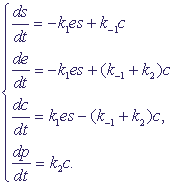 (2) (2)
В системе (2) учтены следующие процессы:
- СубстратS расходуется, образуя комплекс ES (бимолекулярная реакция), и его
концентрация увеличивается при распаде комплекса;
- Фермент E расходуется на образование комплекса ES, его концентрация увеличивается
при распаде комплекса.
- Комплекс ES образуется из фермента E и субстрата S (бимолекулярная реакция)
и распадается на субстрат S и фермент E.
- Продукт P образуется при распаде комплекса.
Для полной математической формулировки задачи Коши необходимо задать начальные
условия:
s0(0) = s0, e(0) = e0, c(0) = 0, p(0) = 0. (3)
Уравнения (2) не являются независимыми. Кроме того, последнее уравнение отделяется от первых трех. Если система первых трех уравнений решена, концентрация продукта может быть рассчитана по формуле:
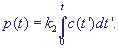
В соответствии со схемой реакций (1-2) общее количество фермента, свободного и связанного в комплекс, сохраняется:
е(t) + с(t) = e0.
Это условие позволяет одно из дифференциальных уравнений системы (2) заменить алгебраическим, и модель сводится к двум дифференциальным уравнениям:
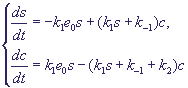 (4) (4)
c начальными условиями: s0(0) = s0 , c(0) = 0.
Введем безразмерные переменные и параметры:
 (5) (5)
Запишем уравнения (4) в безразмерном виде:
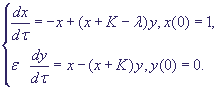 (6) (6)
Из (5) следует, что (К-λ) > 0.
Поскольку реакция превращения фермент-субстратного комплекса необратима, уже из схемы реакций (1) ясно, что с течением времени весь субстрат будет превращен в продукт, и в стационарном состоянии концентрации и субстрата и комплекса станут равны нулю: x = 0, y = 0.
Систему (2) нельзя решить аналитически. Проанализируем качественно, как ведут себя x(t) и y(t).
Вблизи τ = 0 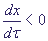 .
Это означает, что x уменьшается от x = 1. В то же время .
Это означает, что x уменьшается от x = 1. В то же время 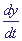 › 0, y растет от y = 0 до величины › 0, y растет от y = 0 до величины 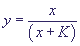 ,
при которой правая часть уравнения для ,
при которой правая часть уравнения для 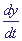 обращается в нуль. После этого величина y будет уменьшаться до нуля. Таким образом, концентрация фермент-субстратного комплекса y проходит через
максимум. В это время величина x (концентрация субстрата) монотонно уменьшается. Относительная концентрация свободного фермента обращается в нуль. После этого величина y будет уменьшаться до нуля. Таким образом, концентрация фермент-субстратного комплекса y проходит через
максимум. В это время величина x (концентрация субстрата) монотонно уменьшается. Относительная концентрация свободного фермента 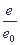 сначала убывает а затем снова возрастает до величины сначала убывает а затем снова возрастает до величины
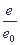 = 1, поскольку с течением времени субстрат исчерпывается, и все меньшая доля фермента оказывается связанной. Кинетические кривые изображены на рис. 1. = 1, поскольку с течением времени субстрат исчерпывается, и все меньшая доля фермента оказывается связанной. Кинетические кривые изображены на рис. 1.
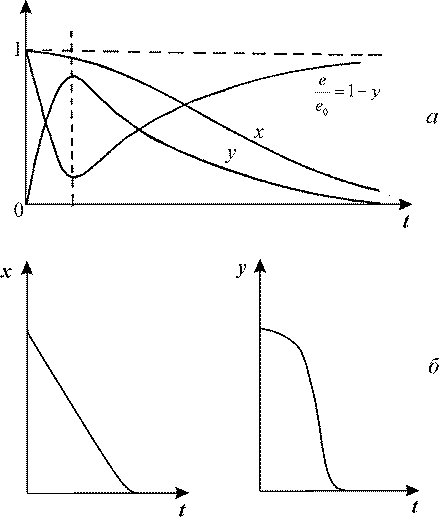
Рис. 1. Кинетика изменения безразмерных переменных в уравнении Михаэлиса-Ментен.
а - с учетом области переходных процессов на малых временах (полная система
6). б - без учета области переходных процессов (редуцированная система 7).
Предположим, что концентрация субстрата значительно превышает
концентрацию фермента: s0 >> e0. Тогда
из соотношений (5) следует, что ε << 1. Если условия Теоремы Тихонова
выполняются (для уравнений Михаэлиса-Ментен это можно показать), мы имеем право
заменить второе из уравнений (6) алгебраическим и найти "квазистационарную концентрацию"
фермент-субстратного комплекса:
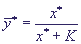 (7) (7)
По терминологии Тихонова, мы получим вырожденную систему:
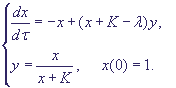 (8) (8)
Подставив выражение для y в дифференциальное уравнение для x, получим:
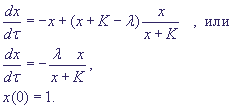
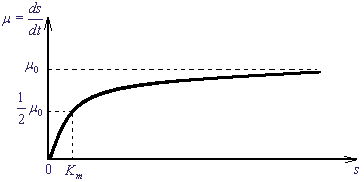
Рис. 2. Закон Михаэлиса - Ментен. Зависимость скорости реакции как функция начальной концентрации субстрата S.
µ0 - максимальная скорость, Km - константа Михаэлиса.
В размерном виде это - классическая формула Михаэлиса - Ментен для кинетики изменения субстрата в ферментативной реакции:
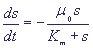 (9) (9)
Таким образом, формула (9) верно отражает изменение концентрации субстрата, но ничего не может сказать об изменении концентраций свободного фермента и фермент-субстратного комплекса, которые на малых временах ведут себя немонотонно (см. рис. 1).
Величина Km называется константой Михаэлиса и имеет размерность концентрации. При s < Km скорость пропорциональна концентрации:
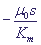 . Она соответствует концентрации субстрата, при которой скорость µ(S) равна половине максимальной. Максимальная скорость ферментативной реакции µ = k2ε0 и зависит линейно от константы скорости стадии распада ферментативного комплекса, которую называют лимитирующей стадией. . Она соответствует концентрации субстрата, при которой скорость µ(S) равна половине максимальной. Максимальная скорость ферментативной реакции µ = k2ε0 и зависит линейно от константы скорости стадии распада ферментативного комплекса, которую называют лимитирующей стадией.
В эксперименте для оценки параметров ферментативной реакции используют кривую зависимости скорости реакции от концентрации субстрата (рис.2, формула 9)
В ферментативных реакциях возможны гораздо более сложные типы динамического поведения: два или несколько устойчивых стационарных состояния, автоколебания, квазистохастические режимы. Они связаны с изменением характера фазового портрета системы, который содержит не одну стационарную точку, а носить более сложный характер.
Генетический триггер Жакоба и Моно
Рассмотрим модель биохимической регуляции белкового синтеза и математически разработанную Д.С. Чернавским в 1967 г. Эта модель показывает принципиальные возможности триггерных систем. Она легла в основу целой серии более подробных и конкретных моделей. Подробный вывод модели описан в книге Романовский Ю.М., Степанова Н.В., Чернавский Д.С. "Математическое моделирование в биофизике. М., 1975.
Схема взаимной регуляции двух систем синтеза ферментов изображена на рис. 3.
Ген-регулятор каждой системы синтезирует неактивный репрессор. Этот репрессор,
соединяясь с продуктом противоположной системы, образует активный комплекс,
который обратимо реагируя с участком структурного гена, называемым опероном,
блокирует синтез мРНК. Таким образом, продукт первой системы P1 является корепрессором второй системы, а продукт второй системы P2 - корепрессором первой. При этом в процессе корепрессии могут принимать участие одна, две и более молекул продукта.
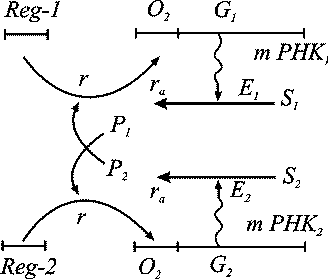
Рис. 3. Схема синтеза двух ферментов
Очевидно, что при таком характере взаимодействий при интенсивной работе первой системы вторая заблокирована, и наоборот. Простейшая система уравнений, описывающая такой тип взаимодействий, имеет вид
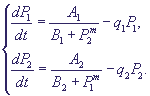 (10) (10)
Здесь P1, P2 - концентрации продуктов, величины A1, A2, B1, B2, выражаются через параметры своих систем. Показатель степени m показывает, сколько молекул активного репрессора (соединений молекул продукта с молекулами неактивного репрессора, который предполагается в избытке) соединяются с опероном для блокировки синтеза матричной РНК.
Введем безразмерные переменные:
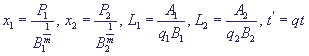 (11) (11)
Опустив штрих у времени, перепишем систему в безразмерном виде:
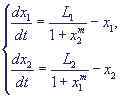 (12) (12)
Исследование системы (12) показало, что при m = 0 фазовый портрет имеет одну устойчивую особую точку в первом квадранте фазовой плоскости (рис. 4, а) и не может описывать процессов переключения в системе.
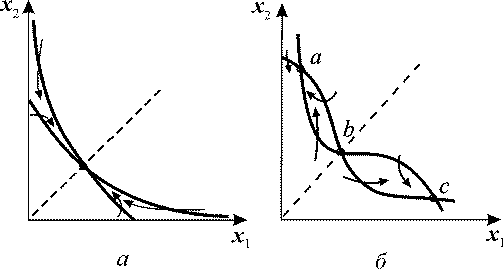
Рис. 4. Главные изоклины на фазовой плоскости системы 12. При m = 1 система
имеет единственное устойчивое стационарное состояние (а). При m = 2 в системе
три стационарных состояния, два из которых (а и с) - устойчивые узлы, а третье
(b) - седло.
При m≥2 и определенных значениях отношения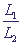 › γ система приобретает триггерные свойства. На фазовой плоскости такая система имеет две устойчивые особые точки, между которыми расположено седло (рис. 4, б). Значение параметра &gamma является бифуркационным, причем
бифуркация имеет триггерный характер (образуется седло). Отношение › γ система приобретает триггерные свойства. На фазовой плоскости такая система имеет две устойчивые особые точки, между которыми расположено седло (рис. 4, б). Значение параметра &gamma является бифуркационным, причем
бифуркация имеет триггерный характер (образуется седло). Отношение 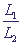 служит управляющим параметром, изменение значения служит управляющим параметром, изменение значения 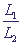 › γ которого может привести к смене стационарного режима в системе, как это было описано выше при рассмотрении параметрического способа переключения системы. Величина параметров L1,L2 зависит от многих
биохимических характеристик: скорости снабжения субстратами, активности ферментов, времени жизни ферментов, мРНК и продуктов и проч. Фазовый портрет триггерной системы 12 приведен на рис. 5. › γ которого может привести к смене стационарного режима в системе, как это было описано выше при рассмотрении параметрического способа переключения системы. Величина параметров L1,L2 зависит от многих
биохимических характеристик: скорости снабжения субстратами, активности ферментов, времени жизни ферментов, мРНК и продуктов и проч. Фазовый портрет триггерной системы 12 приведен на рис. 5.
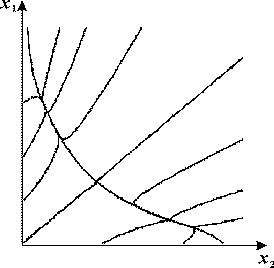
Таким образом, триггерные модели могут описывать процессы отбора и дифференцировки. Подобные механизмы взаимодействия в распределенной системе (при учете пространственной неоднородности и процессов переноса) могут описывать процессы морфогенеза (формообразования).
Колебания в гликолизе
Классическим примером колебательной биохимической реакции является
гликолиз. В процессе гликолиза осуществляется распад глюкозы и других сахаров,
при этом соединения, содержащие шесть молекул углерода, превращаются в трикарбоновые
кислоты, включающие три молекулы углерода. За счет избытка свободной энергии
в процессе гликолиза на одну молекулу шестиуглеродного сахара образуются две
молекулы АТФ. Основную роль в генерации наблюдаемых колебаний концентраций компонентов
реакции: фруктозо-6-фосфата, фруктозо-1,6-фосфата и восстановленного НАД (никотинаминадениндинуклеотид)
играет ключевой фермент гликолитического пути - фосфофруктокиназа (ФФК). Упрощенная
схема реакций представлена на рис. 6:
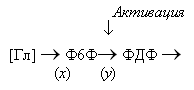
Рис.6. Упрощенная схема реакций гликолиза
На схеме [Гл] - глюкоза, Ф6Ф - фруктозо-6-фосфат - субстрат ключевой реакции,
ФДФ - продукт этой реакции, который является субстратом в следующей стадии. Обе
реакции катализируются ферментами. В безразмерных переменных система описывающих
реакции уравнений может быть записана в виде:
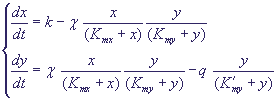
Здесь зависимости скоростей реакций от переменных записаны в форме Михаэлиса-Ментен
(Моно), как это было представлено в уравнении (13). Если выполняются условия:
Kmx>>x, Kmy>>y, можно произвести замену переменных
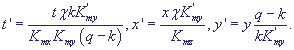
Опустив штрихи у новых переменных, получим систему в безразмерном виде :
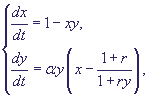 (13) (13)
где
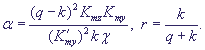
Кинетика изменений переменных и фазовые портреты системы (13) при разных значениях
параметров представлены на рис. 7.
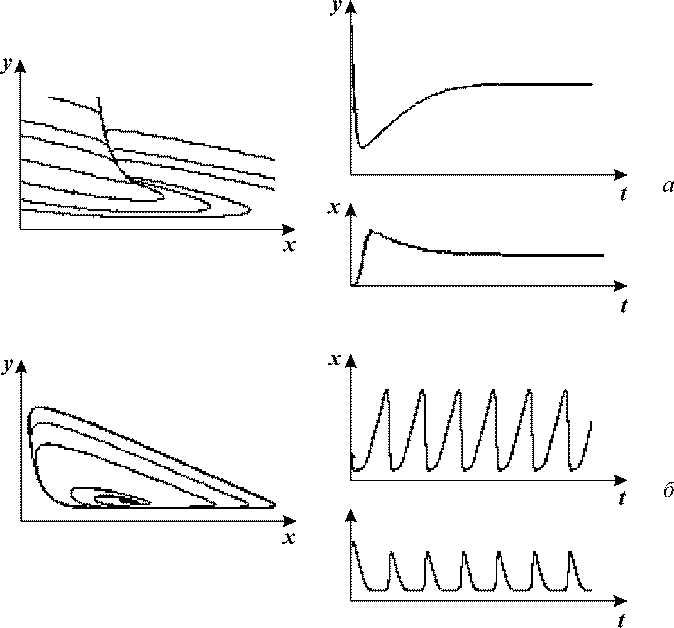
Рис. 7. Модель гликолиза (13). Кинетика изменений концентраций
фруктозо-6-фосфата (х) и фруктозодифосфата (у) (справа) и фазовый
портрет системы (слева) при разных значениях параметров системы,
а - бесколебательный
процесс (узел на фазовой плоскости), α = 0.25; r = 1.
б, г - колебания с постоянной амплитудой
и фазой (предельный цикл на фазовой плоскости), α = 8; r = 0.5.
Интересно, что колебательные реакции в системе гликолиза были сначала предсказаны на математической модели, и лишь
после этого зарегистрированы экспериментально с помощью метода дифференциальной спектрофотометрии.
Внутриклеточные колебания кальция
Во многих типах живых клеток наблюдаются колебания внутриклеточной концентрации
кальция, период которых может варьировать от 0,5 до 10 мин. Простейшая схема процессов, приводящих к гормонально обусловленным колебаниям кальция, основой которых служит кальций индуцированный, выхода кальция из клетки, приведена на рис. 8. Такие колебания впервые наблюдались на клетках скелетных мышц, на клетках саркоплазматического ретикулума сердца быка.
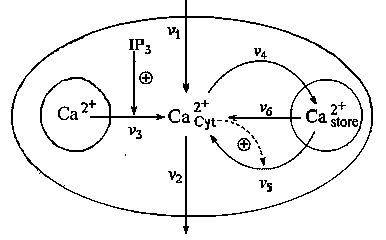
Рис. 8.Схема процессов, приводящих к внутриклеточным колебаниям кальция. IP3 - рецептор, стимулирующий колебания.
Рассматриваются приток и отток кальция в клетку через плазматическую мембрану (константы скоростей v1 и v2, соответственно); гормонально активируемое освобождение кальция из пула (скорость v3); активный транспорт цитозольного кальция в пул, (v4), освобождение кальция из пула, активируемое цитозольным кальцием (v5); свободный отток кальция из пула в цитозоль (v6). Модель состоит из двух дифференциальных уравнений
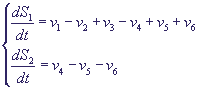 (14) (14)
Здесь S1 концентрация кальция в цитозоле, S2 концентрация кальция в гормонально
чувствительном пуле. Выражения для величин скоростей имеют вид:
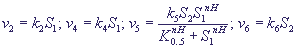 (15) (15)
Модель предсказывает колебания концентрации кальция во времени, по форме близкие к экспериментальным (рис. 9).
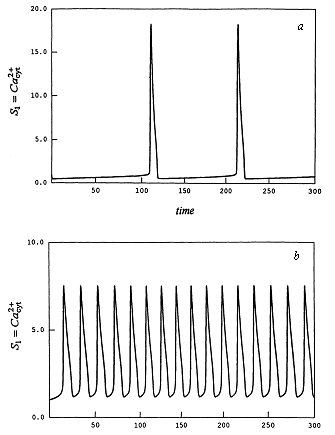
Рис. 9. Модель внутриклеточных колебаний кальция. Кинетика концентрации Ca при разных значениях параметров.
а - k5 = 1, v0 = 1.4,
б - k5 = 1, v0 = 3.0.
Клеточные циклы
В процессе жизненного цикла клетка удваивает свое содержимое и делится на две. В организме млекопитающего для поддержания жизни производятся ежесекундно миллионы новых клеток. Нарушение регуляции пролиферации клеток проявляется как онкологическое
заболевание. Этим вызван большой интерес к изучению и моделированию механизмов регуляции клеточного деления.
Схема клеточного цикла изображена на рис. 10. Клеточный цикл состоит из двух периодов: митоз (М-фаза) включает разделение предварительно удвоенного ядерного материала, деление ядра, деление самой клетки, цитокинез и занимает около часа. Значительно более длительный период между двумя митозами занимает интерфаза,
включающая стадию роста G1, фазу репликации ДНК (S), фазу подготовки к делению
G2. Клеточный цикл (рис.11) регулируется генами и белками-ферментами двух основных классов.
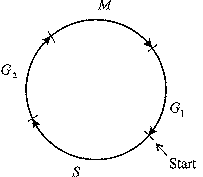
Рис. 10. Схема стадий клеточного цикла
Циклин-зависимые-протеинкиназы (Cdk) индуцируют последовательность процессов
путем фосфорилирования отдельных белков. Циклины, которые синтезируются и деградируют
при каждом новом цикле деления, связываются с молекулами Cdk и контролируют
их способность к фосфорилированию, без циклина Cdk не активны.
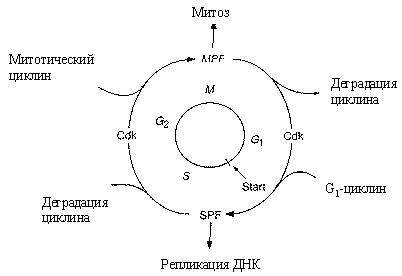
Рис. 11. Схема регуляции клеточного цикла
Количество этих молекул регуляторов различно в разного вида клетках. В делении дрожжевой клетки основные роли играют один Cdk и девять циклинов,
которые образуют девять разных циклин-Cdk комплексов. У гораздо более сложно
организованных млекопитающих изучено шесть Cdk и полтора десятка циклинов. Контроль
выхода клетки из G1-, и G2-фаз осуществляют промотор-фактор S-фазы (SPF) и
промотор-фактор M-фазы (MPF), представляющие собой гетеродимеры. Cуществует особая контрольная
точка клеточного цикла (Start), с которой заканчивается рост (G1-фаза) и начинается
процесс синтеза ДНК.
Постулируется существование фактора транскрипции SBF, который может быть в активной Sa- и пассивной Si -форме. Он переходит в активную форму под действием циклина Cln (N) и Start-киназы (Cdc28-Cln3)
(A) и инактивируется другим веществом (Е). Циклин продуцируется путем активации SBF и деградирует. SBF активируется Chu и Start-киназой и инактивируется фосфатазой. Безразмерная модель процессов имеет вид:
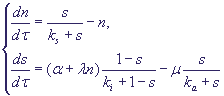 (16) (16)
Модель имеет одно или три стационарных решения (два устойчивых) в зависимости от значений параметров, и при увеличении параметра α в процессе роста клетки описывает переключение системы из G1- в S-фазу.
Добавление двух уравнений сходного вида позволяет описать также переключение из G2 в фазу митоза М. Полная модель, учитывающая и другие регуляторные ферменты в фосфорилированной и дефосфорилированной форме содержит 9 нелинейных уравнений и хорошо описывает кинетику деления ооцитов Xenopus. При соответствующем подборе параметров она применима к описанию деления других типов клеток.
Большое количество работ было посвящено попыткам моделирования периодического
воздействия на клеточный цикл с целью оптимизации параметров рентгено-, радио-
или химиотерапии при воздействии на клетки онкологических опухолей.
В современной литературе по математической биологии рассмотрены сотни автоколебательных
систем на разных уровнях организации живой природы. Несомненно, колебательный
характер процессов - эволюционное изобретение природы, и их функциональная роль
имеет несколько разных аспектов.
Во-первых, колебания позволяют разделить процессы во времени, когда в одном компартменте
клетки протекает сразу несколько различных реакций, организуя периоды высокой и низкой активности отдельных метаболитов. Во-вторых, характеристики колебаний, их амплитуда и фаза, несут определенную информацию и могут играть регуляторную роль в каскадах процессов, проходящих на уровне клетки и живого организма. Наконец, колебательные (потенциально или реально) системы служат локальными элементами распределенных активных сред, способных к пространственно временной самоорганизации, в том числе к процессам морфогенеза.
Модель трансмембранного переноса ионов
Рассмотрим систему переноса ионов К+ и Н+ через клеточную мембрану с участием переносчика Т-. Примером является система К+ - Н+ антипорта с участием нигерицина, у которого имеются места связывания как для протона, так и для калия.
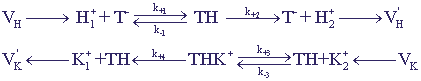
Рис. 12. Схема процессов трансмембранного переноса ионов.
При построении модели используются следующие предположения:
- Приток и отток ионов в систему происходит в примембранных слоях,VH и VK -
скорости притока ионов в сферу реакции.
- Отрицательно заряженный переносчик Т-может переносить протон или ион через
мембрану в форме нейтральных комплексов ТН и ТК или в форме заряженного комплекса
ТНК+.
- Константа связывания для комплекса ТНК+ значительно больше, чем для ТК комплекса,
ион К+ не может вытеснить ион Н+ из ТН комплекса, поэтому его перенос через
мембрану происходит в форме ТНК+.
В соответствии с этими предположениями кинетическая схема процессов может быть
представлена в виде:
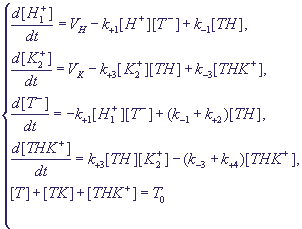 (17) (17)
Здесь Т0 - общая концентрация переносчика в свободной и связанной в комплексы форме.
Индексы 1 и 2 при концентрациях ионов соответствуют примембранному слою
вне и внутри мембраны, k±1,3 - константы ассоциации и диссоциации комплексов,
k2,4 - эффективные константы трансмембранного переноса комплекса и его диссоциации.
Для исследования системы перейдем к безразмерным переменным:
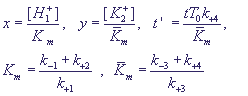 (18) (18)
Введем также безразмерные параметры:
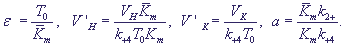 (19) (19)
Пусть концентрация переносчика значительно меньше, чем концентрации ионов в сфере реакции. При этом выполняется неравенство: T0<<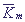 m, которое позволяет
сделать заключение о существовании иерархии времен и провести редукцию системы. А именно, при ε → 0 третье и четвертое уравнения системы (17) можно заменить алгебраическими уравнениями. m, которое позволяет
сделать заключение о существовании иерархии времен и провести редукцию системы. А именно, при ε → 0 третье и четвертое уравнения системы (17) можно заменить алгебраическими уравнениями.
Система уравнений в безразмерных концентрациях протонов (x) и ионов калия (y) примет вид (штрихи при координате времени t и константах скоростей притока ионов в сферу реакции VH, VKопускаем):
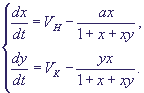 (20) (20)
Система имеет единственное устойчивое стационарное состояние - узел или фокус. Стационарные значения переменных:
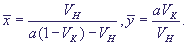 (21) (21)
Линеаризуя систему в окрестности стационарного состояния и решая характеристическое
уравнение, получим условие, при котором особая точка представляет собой фокус:
 (22) (22)
При выполнении этого условия в системе имеют место затухающие колебания. Фазовый портрет системы и кинетика переменных изображены на рис. 13 и 14, а, б, кривые 1.

Рис.13. Фазовый портрет системы (20) при выполнении условия (22) VH = 1, VK=0.96, α = 30.
Наложение низкочастотного периодического поля на рассматриваемую систему приводит к изменению скоростей реакции в системе. В предположении постоянства градиента электрического потенциала в примембранном слое, это влияние можно ввести в уравнения
в виде периодических множителей при константах скоростей притока ионов в сферу реакции, так как величина этих коэффициентов в примембранной области определяется интенсивностью процессов электродиффузии. Приложенное поле слабо влияет на процессы
переноса в самой мембране, поскольку напряженность поля на мембране значительно превосходит напряженность приложенного внешнего поля.
Уравнения с периодически меняющимися коэффициентами имеют вид.
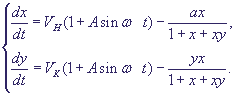 . (23) . (23)
Здесь ω - безразмерная частота воздействия, А - безразмерная амплитуда, показывающая, какую долю напряженности собственного электрического поля в примембранной области составляет напряженность внешнего электрического поля.
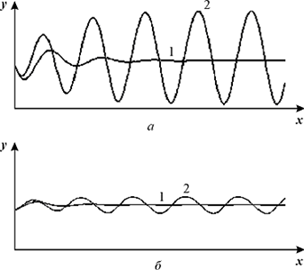
Рис. 14. Изменения безразмерных концентраций (а) - протонов (x) и (б) - ионов
K+ (y) во времени. Кривые 1 - в соответствии с системой уравнений (20), кривые
2 - в соответствии с системой уравнений 23 при периодическом воздействии.
VH = 1, VK = 0.96, α = 30, A = 0.0005, ω = 0.064.
Периодическое воздействие на систему приводит к незатухающим колебаниям переменных, амплитуда которых зависит от частоты внешнего воздействия. На рис. 14 представлены кинетические кривые изменения переменных во времени для системы без внешнего
воздействия - это затухающие колебания (кривые 1) и при внешнем воздействии на "резонансной" частоте (кривые 2) - это незатухающие колебания
Таким образом, рассматриваемая система может работать как усилитель. Под действием слабого низкочастотного поля концентрации ионов начинают меняться периодически. Проведенные оценки показывают, что на резонансной частоте амплитуда этих колебаний может достигать десятых долей (до единицы) pH. Резонансная частота при этом
составляет по разным оценкам от десятых долей до единиц и десятков герц.
Бистабильная модель
Более детальный учет процессов, происходящих в мембране в процессе K - H антипорта, приводит к бистабильной модели. Слабое периодическое воздействие может оказывать существенное влияние на такую систему, причем в качестве управляющего
параметра выступает частота воздействия.
Учтем в схеме 12 возможность образования неактивного комплекса переносчика с двумя ионами водорода
TH+Н+
 (ТН2)+. Схема химических превращений имеет вид:
(ТН2)+. Схема химических превращений имеет вид:
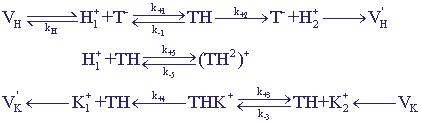
Рис.15. Обозначения те же, что и на схеме 12.
Записывая аналогичную систему кинетических уравнений и произведя редукцию системы
в соответствии с иерархией времен, получим систему уравнений для безразмерных
концентраций протонов и ионов К+:
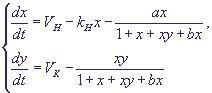 (24) (24)
Безразмерные переменные вводятся по формулам (18), и безразмерные параметры
по формулам (19). Кроме того, в системе появляются еще два безразмерных параметра:
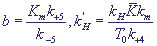 (25) (25)
Стационарное решение может быть получено из уравнений:
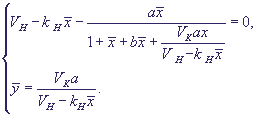 (26) (26)

Рис. 16. Зависимость стационарной концентрации протонов
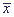 от скорости притока протонов VH (а) и ионов калия VK
(б) в сферу реакции.
от скорости притока протонов VH (а) и ионов калия VK
(б) в сферу реакции.
Стационарная концентрация протонов представляет собой решение уравнения третьей
степени:
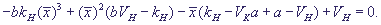 (27) (27)
Уравнение (27) может иметь одно, два или три положительных корня. В последнем
случае два из них являются устойчивыми особыми точками системы (24), а третья,
расположенная между ними - седло.
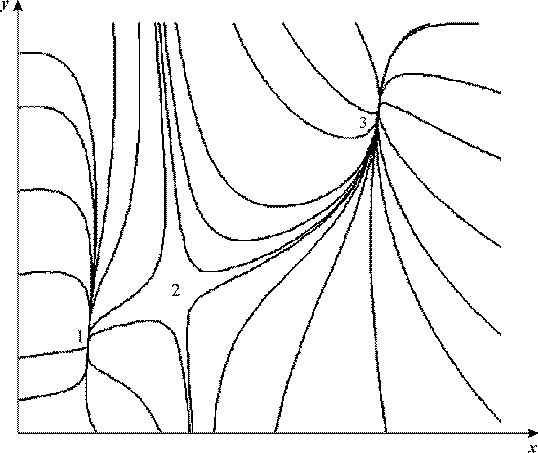
Рис. 17. Фазовый портрет системы 23
VH = 10.637, VK = 0.0325, kH = 1, α = 26.44, b = 0.696
На рис.16, а показана зависимость величины стационарной концентрации
протонов от параметра VH. Существует область значений VH
между VH1 и VH2, в которой имеется три
стационарных решения. Пунктиром обозначена неустойчивая ветвь решений. Зависимость
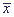 от VК имеет тот же характер (рис. 16, б).
Фазовый портрет системы (26) изображен на рис.17. Стационарные состояния
1,3 - устойчивые узлы, состояние 2 - седло.
от VК имеет тот же характер (рис. 16, б).
Фазовый портрет системы (26) изображен на рис.17. Стационарные состояния
1,3 - устойчивые узлы, состояние 2 - седло.
При периодическом изменении величин VH, VK, аналогично тому, как это было задано
в формуле (24), компьютерный эксперимент показывает следующий результат. Пусть
начальное значение переменных близко к одному из двух стационарных состояний.
При высокой частоте воздействия изображающая точка система колеблется в окрестности,
соответствующей стационарной точке (рис 18, а, кривая 1 или 3).
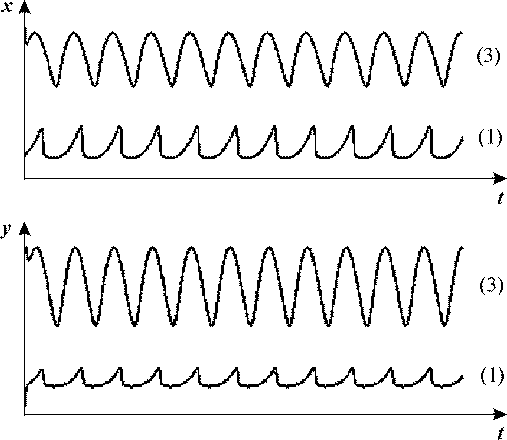
Рис. 18 а. Кинетика изменения переменных в бистабильной системе (24) при
наложении внешнего периодического воздействия.
Для кривых (1) начальные значения переменных соответствуют стационарному состоянию
1 (рис. 17); для кривых (3) - стационарному состоянию 3 (рис. 17). Параметры системы VH = 10.637, VK = 0.0325,
kH = 1, a = 26.44, b = 0.696, амплитуда внешнего воздействия
A = 0.03, частота воздействия ω<ω1.
Будем постепенно уменьшать частоту внешнего воздействия. Существует
некоторое критическое значение частоты ω1, при которой происходит
переход системы в окрестность второго стационарного состояния, где и происходят
дальнейшие колебания (рис.18, б). Для параметров, указанных в подписи к рис.
18, а, значение этой критической частоты ω1 = 0.047.
После достижения следующего критического значения ω2,
(для заданных выше параметров ω2 = 0.023) начинаются колебания
системы между стационарными состояниями 1 и 3 с частотой внешнего воздействия
(рис.18, в). Кинетика переменных для случаев ω1<ω<ω2
(б) и ω>ω2 (в) представлены на рис. 18, б, в:
 Рис. 18, б. ω1<ω<ω2
Рис. 18, б. ω1<ω<ω2
 Рис. 18, в Рис. 18, в
Таким образом, частота внешнего периодического воздействия может служить управляющим
параметром, изменяя который можно переключать систему из одного в другое стационарное
состояние, причем в некотором диапазоне частот это переключение имеет необратимый
характер.
Автоколебательная система
Более детальный учет химических превращений, возможных в системе К+ - Н+ антипорта
приводит к системе, в которой возникают автоколебательные изменения переменных.
Кинетическая схема процессов, кроме учтенных раньше процессов, включает еще
возможность образования неактивного комплекса переносчика с протоном (рис. 19).
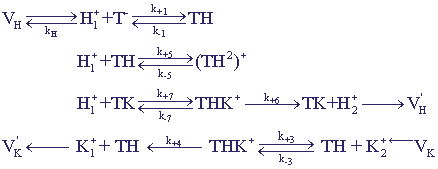
Рис. 19.
Система уравнений в безразмерных переменных (19) c учетом внешнего периодического
воздействия имеет вид:
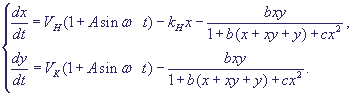 (28) (28)
Кроме введенных в формулах (20), (27) параметров, в формулу (28) входит
также параметр:
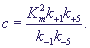 (29) (29)
Исследование системы (28) в отсутствие воздействия (А = 0) показало, что при
определенных значениях параметров выполняется условие теоремы Хопфа , в системе имеет место суперкритическая бифуркация и происходит мягкое рождение предельного цикла. При аналитическом исследовании и компьютерном моделировании
были получены значения управляющего параметра VH, при которых в системе возникают
бифуркационные изменения. Область возникновения бифуркаций является очень узкой: изменения параметра на десятитысячные доли приводит к переходам от режима затухающих колебаний к предельным циклам разной амплитуды и к появлению двух аттракторов,
один из которых устойчивый фокус, а другой - устойчивый предельный цикл большой амплитуды. Изменение структуры фазового портрета в зависимости от величины параметра VH вблизи точки бифуркации Андронова-Хопфа показано на рис. 20.
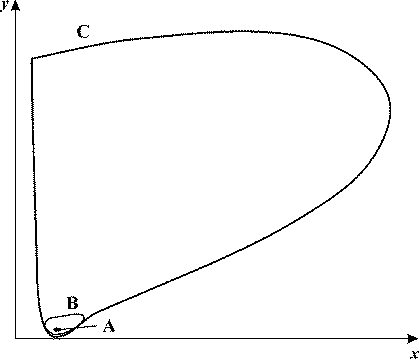
Рис. 20. Фазовый портрет системы (28) в отсутствие внешнего поля (А = 0) при разных значениях параметра VH вблизи значений, соответствующих бифуркации Андронова-Хопфа. x,y - безразмерные
концентрации протонов и ионов калия, VK = 0.5, kH = 0.01, b = 1, c = 1. При VH = 0.5241
в системе реализуется устойчивый фокус А, при VH = 0.5242 возникает предельный
цикл В, при VH = 0.5245 амплитуда цикла резко возрастает, кривая С.
Воздействие внешнего периодического поля на зависящий от градиента потенциала
параметр VH изучали как вблизи точки бифуркации, так и при значениях параметров,
далеких от бифуркации.
Вдали от точек бифуркации система сохраняет устойчивость в широком диапазоне
амплитуд и частот воздействий, характер собственных автоколебаний практически
не меняется.
Вблизи критических значений VH внешнее малое возмущение полем вызывает смену
режима функционирования. При нижнем критическом значении параметраVH = 0.5241,
соответствующем устойчивому фокусу, слабое внешнее воздействие переводит систему
из режима затухающих колебаний в режим автоколебаний. Если воздействие осуществляется,
когда система находится в режиме автоколебаний (при VH, близком к бифуркационному),
в системе возможны переходы от колебаний малой амплитуды к колебаниям большой
амплитуды. На рис. 20 это - переход от цикла B к циклу С. Соответствующая
кинетика переменных показана на рис. 21.
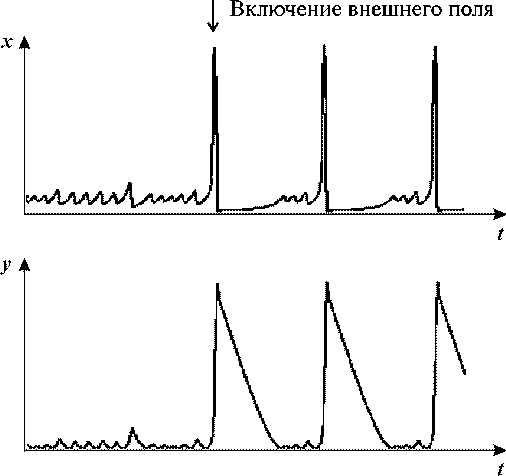
Рис. 21. Кинетика концентраций протонов (x) и
ионов калия (y). В ответ на внешнее периодическое возмущение в системе
возникают переходы от колебаний малой амплитуды к колебаниям большой амплитуды.
VK = 0.5, kH = 0.01, b = 1, c=1, VH = 0.5243, A = 0.0003, ω = 0.004.
Фазовый портрет невозмущенной системы в области больших значений параметра VH
показан на рис. 22.
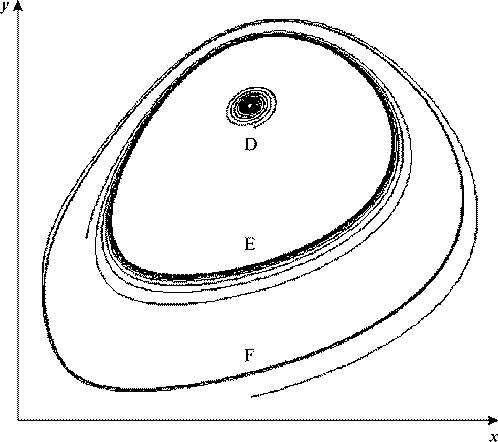
Рис. 22. Фазовый портрет невозмущенной системы вблизи большего критического
значения параметра VH. В интервале значений VH = 0.701÷0.7065 в системе одновременно
существуют устойчивый фокус D, неустойчивый предельный цикл E, устойчивый предельный
цикл F. VK = 0.5, kH = 0.01, b = 1, c =1.
Вблизи верхнего критического значения VH = 0.7065 в ответ на внешнее слабое периодическое
воздействие в зависимости от частоты ответ системы может быть различным. При
относительно высоких частотах воздействия система либо совершает колебания в
окрестности устойчивого фокуса (D на рис. 22), либо стремится к предельному
циклу (F на рис. 22). При некоторых критических частотах систему, находящуюся
вблизи устойчивого фокуса, можно перебросить в окрестность предельного цикла.
Подобное явление переброса от одного аттрактора к другому мы видели в бистабильной
системе.
При уменьшении частоты внешнего воздействия вблизи предельного цикла возникает
предельное множество типа странного аттрактора. Вид траекторий для
значения параметра ω = 0.0025 показан на рис. 23.
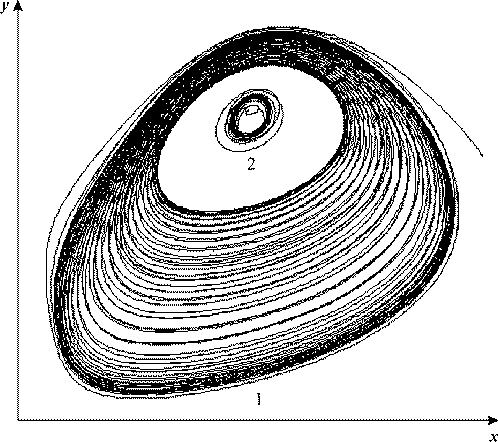
Рис. 23. Квазистохастический режим. VK = 0.5, kH = 0.01, b = 1, c = 1, VH = 0.7065, A = 0.003, ω = 0.0025.
Помимо странного аттрактора при рассматриваемой частоте воздействия в системе
существует предельная периодическая траектория (рис. 23, кривая 2), содержащая
внутри себя неустойчивую точку покоя - неустойчивый фокус. Таким образом, в
системе в зависимости от начальных условий могут реализоваться либо периодические
колебания сравнительно малой амплитуды, либо квазистохастические колебания большой
амплитуды.
Рассмотренная модель является одной из возможных базовых моделей для описания
процессов, возникающих в возбудимых мембранах и других процессов, характеризующихся
набором сложных паттернов поведения.
Все приведенные модели более подробно описаны в книге Г.Ю.Ризниченко "Лекции
по математическим моделям в биологии". М., Изд. РХД, 2002.
К оглавлению
|